การพัฒนานโยบายการเข้าถึงวัคซีนของคนไทย
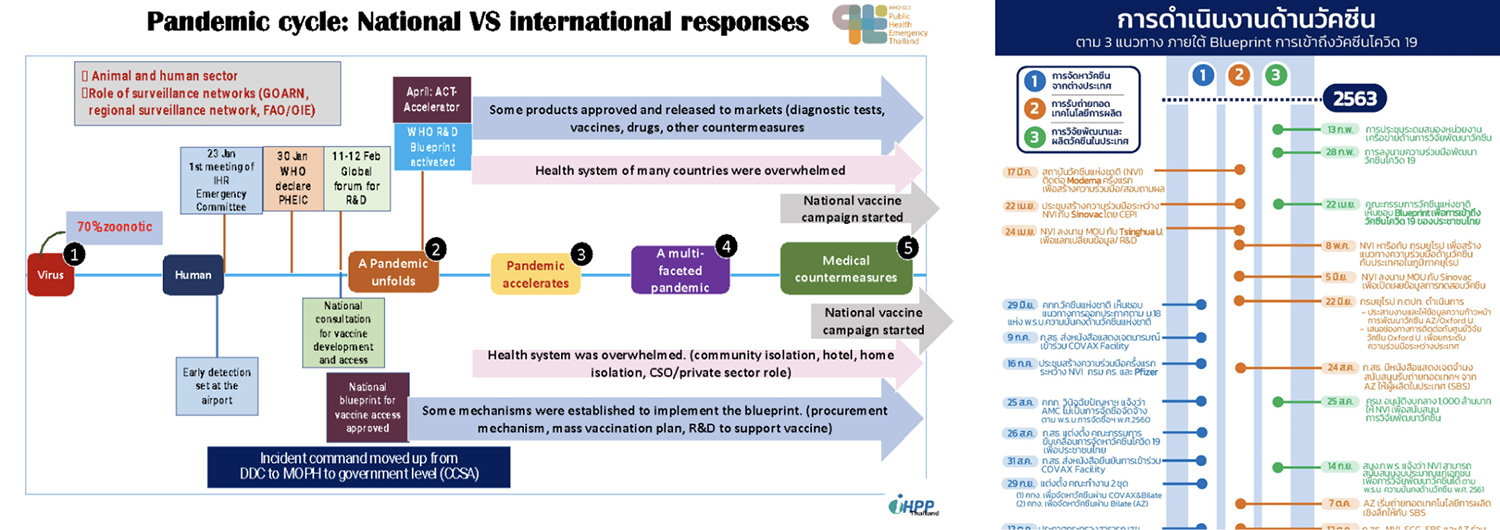
1.1 timeline ที่สำคัญ
กรอบเวลาแสดงภาพรวมของการระบาดและการดำเนินงานสำคัญในระดับนานาชาติและในประเทศไทย ในเดือนธันวาคม พ.ศ. 2562 มีรายงานการระบาดในสาธารณรัฐประชาชนจีนและต่อมามีการประชุม IHR Emergency Committee ในวันที่ 23 มกราคม พ.ศ. 2563 และองค์การอนามัยโลกประกาศว่าการระบาดของโควิด 19 เป็น Public Health Emergency of International Concerns (PHEIC) ในวันที่ 30 มกราคม พ.ศ. 2563
ในเดือนกุมภาพันธ์ พ.ศ. 2563 เป็นเดือนที่มีความเคลื่อนไหวสำคัญของวงการวิทยาศาสตร์และวิจัย ทั้งในระดับโลกและในประเทศไทย มีการจัดประชุมหารือในระดับโลก “2019 novel Corona virus Global research and innovation forum: towards a research roadmap” เพื่อ (1) ประเมินองค์ความรู้ที่มีอยู่ในปัจจุบันของโควิด 19 (2) เห็นชอบคำถามวิจัยสำคัญที่ต้องการคำตอบอย่างเร่งด่วนและวางแนวทางความร่วมมือในการทำงานร่วมกัน รวมถึงการหาแหล่งทุนมาสนับสนุนการวิจัยสำคัญที่ช่วยป้องกันควบคุมการระบาดทั้งในปัจจุบันและในอนาคต โดยเชิญผู้มีส่วนได้ส่วนเสียสำคัญในวงการวิทยาศาสตร์และวิจัยสาขาต่างๆ มาระดมสมองและวางแผนการวิจัยองค์ความรู้ต่างๆ เพื่อแก้ไขปัญหาโควิด 19 รวมถึงการพัฒนา medical countermeasures ต่างๆ ที่สำคัญ โดยเฉพาะยาและวัคซีน [1, 2]
สำหรับในประเทศไทยมีแนวคิดเรื่องการเตรียมการเพื่อเข้าถึงวัคซีนตั้งแต่เริ่มมีการระบาดและมีการจัดประชุมปรึกษาหารือระหว่างผู้เชี่ยวชาญในประเทศภายหลังจากการประชุม global consultation 1 วัน ในวันที่ 13 กุมภาพันธ์ 2563 โดยนำข้อมูลและข้อสรุปที่สำคัญจาก global consultation มาเป็นข้อมูลประกอบการประชุม ผลการประชุมในประเทศไทยเห็นว่าประเทศไทยควรมีนโยบายเร่งด่วนที่จะให้คนไทยเข้าถึงวัคซีนโควิด 19 โดยควรมีทั้งการวิจัยและพัฒนาวัคซีนเองและการจัดซื้อจัดหาวัคซีนจากต่างประเทศ
เริ่มตั้งแต่มีนาคม 2563 เป็นต้นมา สถาบันวัคซีนแห่งชาติและกรมควบคุมโรค ได้ติดต่อ กับผู้ผลิตวัคซีนในต่างประเทศ เพื่อพูดคุยในการสร้างความร่วมมือสำหรับการวิจัยและพัฒนาผลิต และการเตรียมการสำหรับการจัดซื้อจัดหาวัคซีน (โมเดอร์นา ซิโนแวค COVAX Facility Pfizer)
เมษายน พ.ศ. 2563 คณะกรรมการวัคซีนแห่งชาติเห็นชอบ Blueprint เพื่อการเข้าถึงวัคซีนป้องกันโควิด 19 ของประชาชนไทย เมื่อวันที่ 22 เมษายน 2563 ซึ่งมีแนวทางการเข้าถึงวัคซีน 3 แนวทางได้แก่ 1) การวิจัยและพัฒนาวัคซีนในประเทศ 2) การรับถ่ายทอดเทคโนโลยีจากต่างประเทศเพื่อผลิต 3) การจัดซื้อจัดหาวัคซีนจากต่างประเทศ
12-14 พฤษภาคม 2563 สถาบันวัคซีนแห่งชาติ พร้อมผู้เชี่ยวชาญจากหน่วยงานเครือข่าย ผู้แทนจากสำนักงานคณะกรรมการอาหารและยา (อย.) กรมวิทยาศาสตร์การแพทย์ และผู้เชี่ยวชาญจากองค์การอนามัยโลก (WHO) ได้ศึกษาดูงานหน่วยงานผู้ผลิตในประเทศเพื่อเตรียมความพร้อมร่วมกัน
มิถุนายน ถึง กรกฎาคม 2563 มีการหารือระดับนโยบายหลายครั้งเพื่อเตรียมการจัดซื้อจัดหาวัคซีน โดยเฉพาะประเด็นข้อกฎหมายที่เกี่ยวข้องกับการจองซื้อวัคซีนล่วงหน้า (AMC: Advanced Market Commitment) ได้แก่ ประเด็นการจองซื้อวัคซีนเข้าข่ายตามพระราชบัญญัติจัดซื้อจัดจ้างหรือไม่ และ หากไม่เข้าข่าย จะมีข้อกฎหมายใดรองรับการจองซื้อวัคซีนล่วงหน้า
25 สิงหาคม 2563 คณะกรรมการวินิจฉัยปัญหาฯ แจ้งว่า AMC ไม่เป็นการจัดซื้อจัดจ้างตามพระราชบัญญัติจัดซื้อจัดจ้างฯ
25 สิงหาคม 2563 ครม. อนุมัติงบกลาง 1,000 ล้านบาท เพื่อสนับสนุนการวิจัยและพัฒนาวัคซีนในประเทศไทย
26 สิงหาคม 2563 กระทรวงสาธารณสุขแต่งตั้งคณะกรรมการขับเคลื่อนการจัดหาวัคซีนโควิด 19 เพื่อประชาชนไทย และมีการประชุมต่อเนื่องเพื่อวางแผนจัดซื้อจัดหาวัคซีนโควิด 19
7 ตุลาคม 2563 AstraZeneca เริ่มถ่ายทอดเทคโนโลยีการผลิตเชิงลึกให้แก่ SBS
12 ตุลาคม 2563 กระทรวงสาธารณสุข สถาบันวัคซีนแห่งชาติ บริษัทสยามซีเมนต์กรุ๊ป และบริษัทแอสตราเซเนนกา ได้ลงนามบันทึกความร่วมมือ ในการผลิต และจัดสรรวัคซีน ชนิดไวรัลเวกเตอร์ในประเทศไทย
12 ตุลาคม 2563 ประกาศกระทรวงสาธารณสุข เรื่องการจัดหาวัคซีนโควิด 19 กรณีมีเหตุฉุกเฉินจำเป็น พ.ศ. 2563
17 พฤศจิกายน 2563 ครม. เห็นชอบโครงการจัดหาวัคซีนโควิด 19 แบบ AMC จากแอสตร้าเซเนนก้า
17 ธันวาคม 2563 การลงนามในบันทึกความร่วมมือระหว่างสถาบันวัคซีนแห่งชาติ และบริษัทสยามไบโอไซเอนซ์ในการพัฒนาการผลิตวัคซีนป้องกันโรคติดเชื้อไวรัสโคโรนา 2019 (COVID-19)
18 ธันวาคม 2563 บริษัท สยามไบโอไซเอนซ์ จำกัด ได้ลงนามในสัญญารับทุนอุดหนุนโครงการเตรียมความพร้อมเพื่อรองรับการผลิตวัคซีนโควิด 19 ชนิด Adenovirus ในระดับ 2,000 ลิตร งบประมาณจำนวนทั้งสิ้น 596.23 ล้านบาท จากสถาบันวัคซีนแห่งชาติ
29 ธันวาคม 2563 ครม. อนุมัติงบวิจัยและพัฒนาวัคซีนภายใต้ พ.ร.ก. กู้เงิน พ.ศ. 2563 วงเงิน 1,810 ล้านบาท
5 มกราคม 2564 ครม. เห็นชอบกรอบงบประมาณการจัดหาวัคซีนโควิด 19 (SINOVAC) จำนวน 2 ล้านโด๊ส
20 มกราคม 2564 วัคซีน COVID-19 VACCINE ASTRAZENECA ขึ้นทะเบียนโดยสำนักงานคณะกรรมการอาหารและยา
24 กุมภาพันธ์ 2564 วัคซีนส่งถึงประเทศไทยครั้งแรก (AZ 117,000 doses SV 200,000 doses)
28 กุมภาพันธ์ 2564 ประเทศไทยเริ่มฉีดวัคซีนครั้งแรก
2 มิถุนายน 2564 ประเทศไทยได้รับวัคซีนโควิด 19 ชุดแรกที่ผลิตโดยบริษัท สยามไบโอไซเอนท์ จำกัด
1.2 Lorem
กรอบเวลาแสดงภาพรวมของการระบาดและการดำเนินงานสำคัญในระดับนานาชาติและในประเทศไทย ในเดือนธันวาคม พ.ศ. 2562 มีรายงานการระบาดในสาธารณรัฐประชาชนจีนและต่อมามีการประชุม IHR Emergency Committee ในวันที่ 23 มกราคม พ.ศ. 2563 และองค์การอนามัยโลกประกาศว่าการระบาดของโควิด 19 เป็น Public Health Emergency of International Concerns (PHEIC) ในวันที่ 30 มกราคม พ.ศ. 2563
ในเดือนกุมภาพันธ์ พ.ศ. 2563 เป็นเดือนที่มีความเคลื่อนไหวสำคัญของวงการวิทยาศาสตร์และวิจัย ทั้งในระดับโลกและในประเทศไทย มีการจัดประชุมหารือในระดับโลก “2019 novel Corona virus Global research and innovation forum: towards a research roadmap” เพื่อ (1) ประเมินองค์ความรู้ที่มีอยู่ในปัจจุบันของโควิด 19 (2) เห็นชอบคำถามวิจัยสำคัญที่ต้องการคำตอบอย่างเร่งด่วนและวางแนวทางความร่วมมือในการทำงานร่วมกัน
รวมถึงการหาแหล่งทุนมาสนับสนุนการวิจัยสำคัญที่ช่วยป้องกันควบคุมการระบาดทั้งในปัจจุบันและในอนาคต โดยเชิญผู้มีส่วนได้ส่วนเสียสำคัญในวงการวิทยาศาสตร์และวิจัยสาขาต่างๆ มาระดมสมองและวางแผนการวิจัยองค์ความรู้ต่างๆ เพื่อแก้ไขปัญหาโควิด 19 รวมถึงการพัฒนา medical countermeasures ต่างๆ ที่สำคัญ โดยเฉพาะยาและวัคซีน [1, 2]
สำหรับในประเทศไทยมีแนวคิดเรื่องการเตรียมการเพื่อเข้าถึงวัคซีนตั้งแต่เริ่มมีการระบาดและมีการจัดประชุมปรึกษาหารือระหว่างผู้เชี่ยวชาญในประเทศภายหลังจากการประชุม global consultation 1 วัน ในวันที่ 13 กุมภาพันธ์ 2563 โดยนำข้อมูลและข้อสรุปที่สำคัญจาก global consultation มาเป็นข้อมูลประกอบการประชุม ผลการประชุมในประเทศไทยเห็นว่าประเทศไทยควรมีนโยบายเร่งด่วนที่จะให้คนไทยเข้าถึงวัคซีนโควิด 19 โดยควรมีทั้งการวิจัยและพัฒนาวัคซีนเองและการจัดซื้อจัดหาวัคซีนจากต่างประเทศ
เริ่มตั้งแต่มีนาคม 2563 เป็นต้นมา สถาบันวัคซีนแห่งชาติและกรมควบคุมโรค ได้ติดต่อ กับผู้ผลิตวัคซีนในต่างประเทศ เพื่อพูดคุยในการสร้างความร่วมมือสำหรับการวิจัยและพัฒนาผลิต และการเตรียมการสำหรับการจัดซื้อจัดหาวัคซีน (โมเดอร์นา ซิโนแวค
| JEE | GHS Index |
|---|---|
| องค์การอนามัยโลก | NTI และ John Hopkins University |
| เพื่อประเมินขีดความสามารถของรัฐสมาชิกภายใต้ IHR 2005 ตาม IHR core capacities ใน 19 สาขา (technical areas) | เพื่อประเมินขีดความสามารถของรัฐสมาชิกภายใต้ IHR 2005 ใน 11 สาขา (Action packages) |
| All hazard approach |
สุขภาพ เช่น การวิจัย การขนส่ง โครงสร้างพื้นฐานที่เกี่ยวข้องกับ การสื่อสาร คำมั่นในการพัฒนาระบบความมั่นคงด้านสุขภาพใน ระดับสูง ความมั่นคงทางการเมืองและเศรษฐกิจ/สังคม ความไม่ สงบทางสังคม |
| เป็นการประเมินร่วมกันระหว่างทีมภายนอกและทีมของประเทศ โดยเห็นชอบร่วมกันกับผลการประเมิน และการประเมินเป็นไป ตามความสมัครใจ | เป็นการประเมิน |
| คาดหวังไว้ทุก 5 ปี | ทุก 2 ปี |